Questões de química
Origem: Fuvest
(Fuvest-2014) A tabela abaixo apresenta informações sobre cinco gases contidos em recipientes separados e selados.
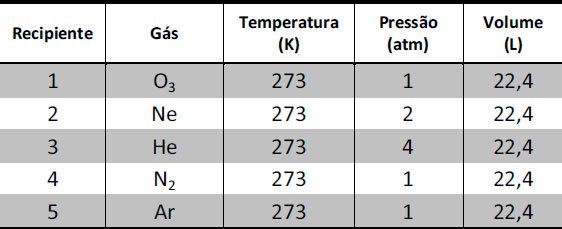
Qual recipiente contém a mesma quantidade de átomos que um recipiente selado de 22,4 L, contendo H2, mantido a 2 atm e 273 K?
a)1
b)2
c)3
d)4
e)5
 resposta:
resposta:C.

(Fuvest-2014) No processo tradicional, o etanol é produzido a partir do caldo da cana-de-açúcar por fermentação promovida por leveduras naturais, e o bagaço
de cana é desprezado.
Atualmente, leveduras geneticamente modificadas podem ser utilizadas em novos processos de fermentação para a produção de biocombustíveis. Por
exemplo, no processo A, o bagaço de cana, após hidrólise da celulose e da hemicelulose, também pode ser transformado em etanol.
No processo B, o caldo de cana, rico em sacarose, é transformado em farneseno que, após hidrogenação das ligações duplas, se transforma no
"diesel de cana". Esses três processos de produção de biocombustíveis podem ser representados por:
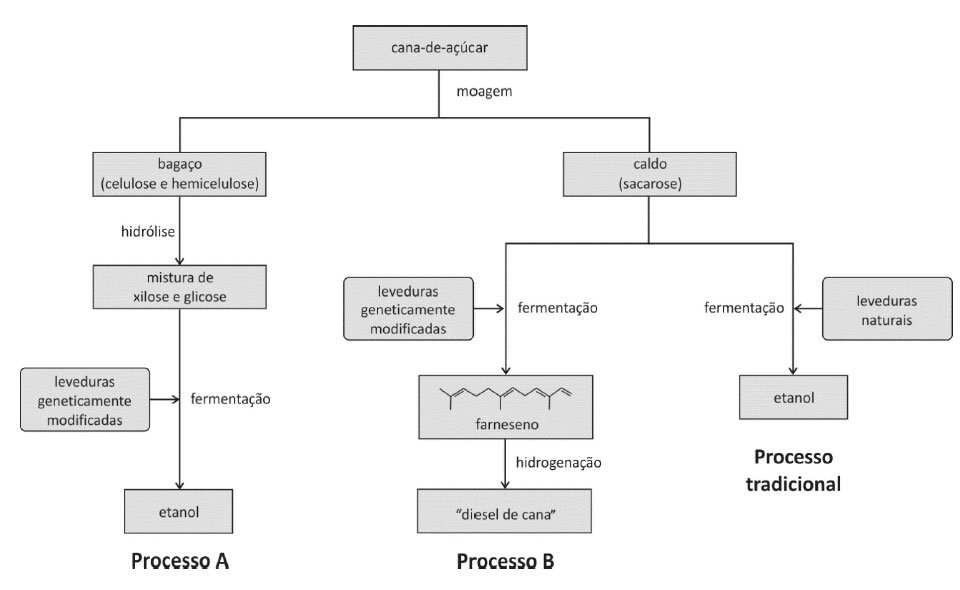
Com base no descrito acima, é correto afirmar:
a)No Processo A, a sacarose é transformada em celulose por micro-organismos transgênicos.
b)O Processo A, usado em conjunto com o processo tradicional, permite maior produção de etanol por hectare cultivado.
c)O produto da hidrogenação do farneseno não deveria ser chamado de “diesel”, pois não é um hidro caboneto,
d)A combustão do etanol produzido por micro-orgnismos transgênicos não é poluente, pois não produz dióxido de carbono.
e)O Processo B é vantajoso em relação ao Processo A, pois a sacarose é matéria-prima com menor valor ecnômico do que o bagaço de cana.
 resposta:
resposta:B.

(Fuvest-2011) As fórmulas estruturais de alguns componentes de
óleos essenciais, responsáveis pelo aroma de certas
ervas e flores, são:
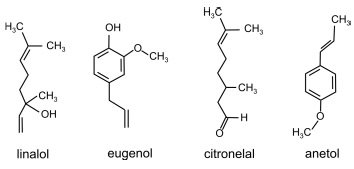
Dentre esses compostos, são isômeros:
a) anetol e linalol.
b) eugenol e linalol.
c) citronelal e eugenol.
d) linalol e citronelal.
e) eugenol e anetol.
 resposta:
resposta:[D]

(Fuvest-2014) Uma embalagem de sopa instantânea apresenta, entre outras, as seguintes informações: “Ingredientes: tomate, sal, amido, óleo vegetal,
emulsificante, conservante, flavorizante, corante, antioxidante”. Ao se misturar o conteúdo da embalagem com água quente, poderia ocorrer a
separação dos componentes X e Y da mistura, formando duas fases, caso o ingrediente Z não estivesse presente.
Assinale a alternativa em que X, Y e Z estão corretamente identificados.
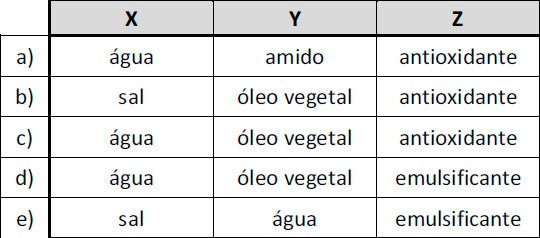
 resposta:
resposta:B.

(Fuvest-2011) Em cadeias carbônicas, dois átomos de carbono
podem formar ligação simples (C?C), dupla (C?C) ou
tripla (C?C). Considere que, para uma ligação simples,
a distância média de ligação entre os dois átomos de
carbono é de 0,154 nm, e a energia média de ligação é
de 348 kJ/mol.
Assim sendo, a distância média de ligação (d) e a
energia média de ligação (E), associadas à ligação
dupla (C?C), devem ser, respectivamente,
a) d < 0,154 nm e E > 348 kJ/mol.
b) d < 0,154 nm e E < 348 kJ/mol.
c) d = 0,154 nm e E = 348 kJ/mol.
d) d > 0,154 nm e E < 348 kJ/mol.
e) d > 0,154 nm e E > 348 kJ/mol.
 resposta:
resposta:[A]

(Fuvest-2014) Em um laboratório químico, um estudante encontrou quatro frascos (1, 2, 3 e 4) contendo soluções aquosas incolores de sacarose, KCl, HCl e
NaOH, não necessariamente nessa ordem. Para identificar essas soluções, fez alguns experimentos simples, cujos resultados são apresentados na
tabela a seguir:

As soluções aquosas nos frascos 1, 2, 3 e 4 são, respectivamente, de
a)HCl, NaOH, KCl e sacarose.
b)KCl, NaOH, HCl e sacarose.
c)HCl, sacarose, NaOH e KCl.
d)KCl, sacarose, HCl e NaOH.
e)NaOH, HCl, sacarose e KCl.
 resposta:
resposta:B.

(Fuvest-2011) Para investigar o fenômeno de oxidação do ferro,
fez-se o seguinte experimento: No fundo de cada um de
dois tubos de ensaio, foi colocada uma amostra de fios
de ferro, formando uma espécie de novelo. As duas
amostras de ferro tinham a mesma massa. O primeiro
tubo foi invertido e mergulhado, até certa altura, em um
recipiente contendo água. Com o passar do tempo,
observou-se que a água subiu dentro do tubo, atingindo
seu nível máximo após vários dias. Nessa situação,
mediu-se a diferença (x) entre os níveis da água no tubo
e no recipiente. Além disso, observou-se corrosão
parcial dos fios de ferro. O segundo tubo foi mergulhado
em um recipiente contendo óleo em lugar de água.
Nesse caso, observou-se que não houve corrosão
visível do ferro e o nível do óleo, dentro e fora do tubo,
permaneceu o mesmo.

Sobre tal experimento, considere as seguintes
afirmações:
I. Com base na variação (x) de altura da coluna de
água dentro do primeiro tubo de ensaio, é possível
estimar a porcentagem de oxigênio no ar.
II. Se o experimento for repetido com massa maior de
fios de ferro, a diferença entre o nível da água no
primeiro tubo e no recipiente será maior que x.
III. O segundo tubo foi mergulhado no recipiente com
óleo a fim de avaliar a influência da água no
processo de corrosão.
Está correto o que se afirma em
a) I e II, apenas.
b) I e III, apenas.
c) II, apenas.
d) III, apenas.
e) I, II e III.
 resposta:
resposta:[B]

(Fuvest-2011) Uma das consequências do “efeito estufa” é o
aquecimento dos oceanos. Esse aumento de
temperatura provoca
a) menor dissolução de CO2 nas águas oceânicas, o
que leva ao consumo de menor quantidade desse
gás pelo fitoplâncton, contribuindo, assim, para o
aumento do efeito estufa global.
b) menor dissolução de O2 nas águas oceânicas, o que
leva ao consumo de maior quantidade de CO2 pelo
fitoplâncton, contribuindo, assim, para a redução do
efeito estufa global.
c) menor dissolução de CO2 e O2 nas águas
oceânicas, o que leva ao consumo de maior
quantidade de O2 pelo fitoplâncton, contribuindo,
assim, para a redução do efeito estufa global.
d) maior dissolução de CO2 nas águas oceânicas, o
que leva ao consumo de maior quantidade desse
gás pelo fitoplâncton, contribuindo, assim, para a
redução do efeito estufa global.
e) maior dissolução de O2 nas águas oceânicas, o que
leva à liberação de maior quantidade de CO2 pelo
fitoplâncton, contribuindo, assim, para o aumento do
efeito estufa global.
 resposta:
resposta:[A]

(Fuvest-2013) (FUVEST-2013)A partir de considerações teóricas, foi feita uma estimativa do poder calorífico (isto é, da
quantidade de calor liberada na combustão completa de 1 kg de combustível) de grande número de hidrocarbonetos.
Dessa maneira, foi obtido o seguinte gráfico de valores
teóricos:
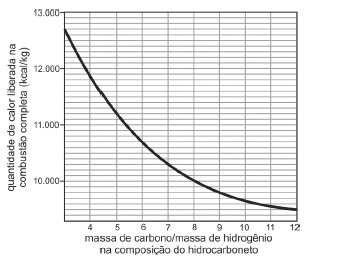
Com base no gráfico, um hidrocarboneto que libera 10.700 kcal/kg em sua combustão completa pode ser representado
pela fórmula
a) CH4
b) C2H4
c) C4H10
d) C5H8
e) C6H6
Dados:
Massas molares (g/mol) C = 12,0
H = 1,00
 resposta:
resposta:Alternativa B.

(Fuvest-2014) Estudos recentes parecem indicar que o formato do olho humano e a visão são influenciados pela quantidade da substância X, sintetizada pelo
organismo. A produção dessa substância é favorecida pela luz solar, e crianças que fazem poucas atividades ao ar livre tendem a desenvolver
dificuldade para enxergar objetos distantes. Essa disfunção ocular é comumente chamada de miopia.
Considere a fórmula estrutural da substância X e os diferentes formatos de olho:
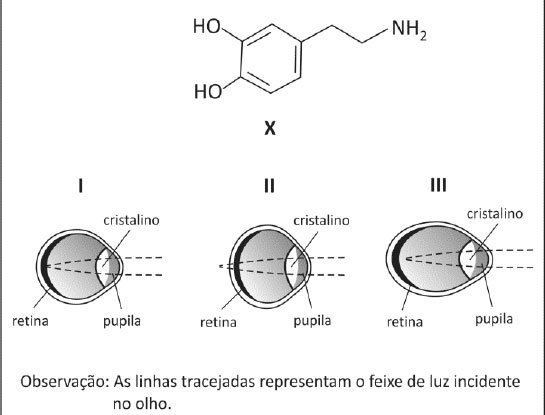
Observação: As linhas tracejadas representam o feixe de luz incidente no olho.
Com base nessas informações, conclui-se que a miopia poderá atingir crianças cujo organismo venha a produzir________ X em quantidade
insuficiente, levando à formação de olho do tipo _______________
As lacunas da frase acima devem ser preenchidas, respectivamente, por
a)o aminoácido; III.
b)a amina; II.
c)o aminoácido; I.
d)o fenol; I.
e)a amina; III.
 resposta:
resposta:E.

(Fuvest-2011) Água e etanol misturam-se completamente, em
quaisquer proporções. Observa-se que o volume final
da mistura é menor do que a soma dos volumes de
etanol e de água empregados para prepará-la. O gráfico
a seguir mostra como a densidade varia em função da
porcentagem de etanol (em volume) empregado para
preparar a mistura (densidades medidas a 20 oC).
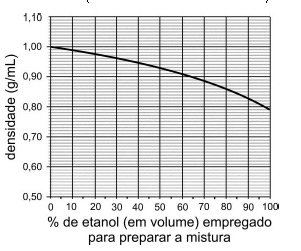
Se 50 mL de etanol forem misturados a 50 mL de água,
a 20 oC, o volume da mistura resultante, a essa mesma
temperatura, será de, aproximadamente,
a) 76 mL
b) 79 mL
c) 86 mL
d) 89 mL
e) 96 mL
 resposta:
resposta:[E]

(Fuvest-2014) A adição de um soluto à água altera a temperatura de ebulição desse solvente. Para quantificar essa variação em função da concentração e da
natureza do soluto, foram feitos experimentos, cujos resultados são apresentados abaixo. Analisando a tabela, observa-se que a variação de
temperatura de ebulição é função da concentração de moléculas ou íons de soluto dispersos na solução
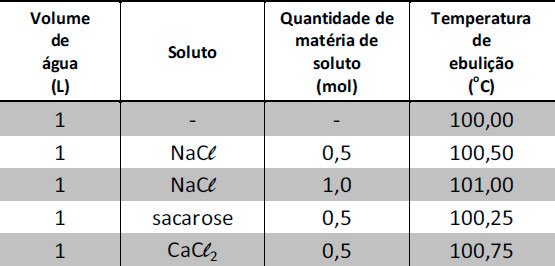
Dois novos experimentos foram realizados, adicionando-se 1 mol de Na2SO4 a 1 L de água (experimento A) e 1,0 mol de glicose a 0,5 L de água
(experimento B). Considere que os resultados desses novos experimentos tenham sido consistentes com os experimentos descritos na tabela.
Assim sendo, as temperaturas de ebulição da água, em °C, nas soluções dos experimentos A e B, foram, respectivamente, de
a)100,25 e 100,25.
b)100,75 e 100,25.
c)100,75 e 100,50.
d)101,50 e 101,00.
e)101,50 e 100,50.
 resposta:
resposta:D.

(Fuvest-2013) (FUVEST-2013)O ácido gama-hidroxibutírico é utilizado no tratamento do alcoolismo. Esse ácido pode ser obtido a
partir da
gamabutirolactona, conforme a representação a seguir:
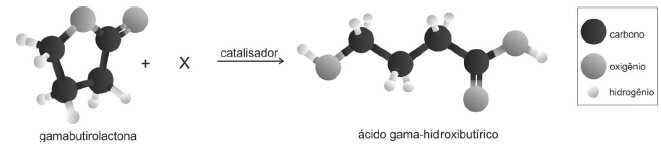
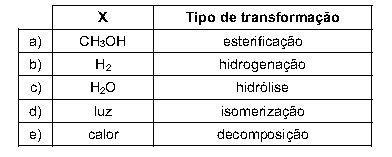
Assinale a alternativa que identifica corretamente X (de modo que a representação respeite a conservação da
matéria) e o tipo de transformação que ocorre quando a gamabutirolactona é convertida no ácido
gamahidroxibutírico.

 resposta:
resposta:Alternativa C.

(Fuvest-2013) (FUVEST-2013)A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa
temperatura, o equilíbrio entre as três substâncias foi estudado, em recipientes fechados, partindo-se de uma
mistura equimolar de H2 e I2 (experimento A) ou somente de HI (experimento B).
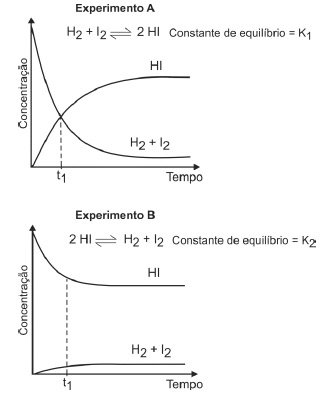
Pela análise dos dois gráficos, pode-se concluir que:
a) no experimento A, ocorre diminuição da pressão
total no interior do recipiente, até que o equilíbrio
seja atingido.
b) no experimento B, as concentrações das
substâncias (HI, H2 e I2) são iguais no instante t1.
c) no experimento A, a velocidade de formação de HI
aumenta com o tempo.
d) no experimento B, a quantidade de matéria (em
mols) de HI aumenta até que o equilíbrio seja
atingido.
e) no experimento A, o valor da constante de equilíbrio
(K1) é maior do que 1.
 resposta:
resposta:Alternativa E.

(Fuvest-2013) (FUVEST-2013)Quando certos metais são colocados em contato com soluções ácidas, pode haver formação de gás
hidrogênio. Abaixo, segue uma tabela elaborada por uma estudante de Química, contendo resultados de experimentos
que ela realizou em diferentes condições.
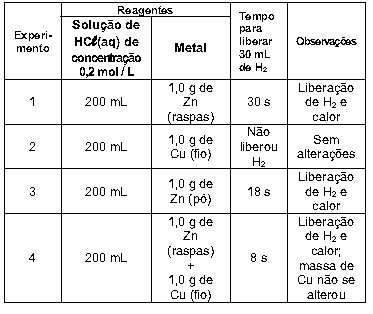
Após realizar esses experimentos, a estudante fez três
afirmações:
I. A velocidade da reação de Zn com ácido aumenta
na presença de Cu.
II. O aumento na concentração inicial do ácido causa o aumento da velocidade de liberação do gás H2.
III. Os resultados dos experimentos 1 e 3 mostram que, quanto maior o quociente superfície de contato/massa
total de amostra de Zn, maior a velocidade de reação.
Com os dados contidos na tabela, a estudante somente
poderia concluir o que se afirma em
a) I.
b) II.
c) I e II.
d) I e III.
e) II e III.
 resposta:
resposta:Alternativa D.

(Fuvest-2013) (FUVEST-2013)Um aluno estava analisando a Tabela Periódica e
encontrou vários conjuntos de três elementos químicos
que apresentavam propriedades semelhantes.
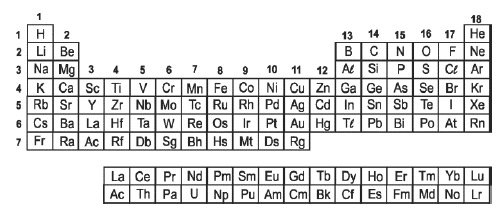
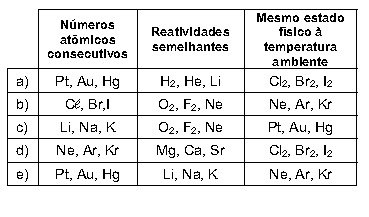
Assinale a alternativa na qual os conjuntos de três elementos ou substâncias elementares estão corretamente
associados às propriedades indicadas no quadro abaixo.
 resposta:
resposta:Alternativa E.

(Fuvest-2014) O rótulo de uma lata de desodorante em aerosol apresenta, entre outras, as seguintes informações: “Propelente: gás butano. Mantenha longe do
fogo”. A principal razão dessa advertência é:
a)O aumento da temperatura faz aumentar a pressão do gás no interior da lata, o que pode causar uma explosão.
b)A lata é feita de alumínio, que, pelo aquecimento, pode reagir com o oxigênio do ar.
c)O aquecimento provoca o aumento do volume da lata, com a consequente condensação do gás em seu interior.
d)O aumento da temperatura provoca a polimerização do gás butano, inutilizando o produto.
e)A lata pode se derreter e reagir com as substâncias contidas em seu interior, inutilizando o produto.
 resposta:
resposta:A.

(Fuvest-2013) (FUVEST-2013)O craqueamento catalítico é um processo utilizado na indústria petroquímica para converter
algumas frações do petróleo que são mais pesadas (isto é, constituídas por compostos de massa molar elevada) em
frações mais leves, como a gasolina e o GLP, por
exemplo. Nesse processo, algumas ligações químicas nas moléculas de grande massa molecular são rompidas, sendo
geradas moléculas menores.
A respeito desse processo, foram feitas as seguintes
afirmações:
I. O craqueamento é importante economicamente, pois converte frações mais pesadas de petróleo em compostos de
grande demanda.
II. O craqueamento libera grande quantidade de energia, proveniente da ruptura de ligações químicas nas
moléculas de grande massa molecular.
III. A presença de catalisador permite que as transformações químicas envolvidas no craqueamento ocorram mais
rapidamente.
Está correto o que se afirma em
a) I, apenas.
b) II, apenas.
c) I e III, apenas.
d) II e III, apenas.
e) I, II e III.
 resposta:
resposta:Alternativa C.

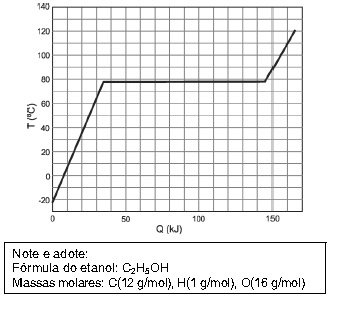
(Fuvest-2013) (FUVEST-2013)Em um recipiente termicamente isolado e mantido a pressão constante, são colocados 138 g de
etanol líquido. A seguir, o etanol é aquecido e sua temperatura T é medida como função da quantidade de calor Q a
ele transferida. A partir do gráfico de TxQ, apresentado na figura abaixo, pode-se determinar o calor específico
molar para o estado líquido e o calor latente molar de vaporização do etanol como sendo, respectivamente,
próximos de
a) 0,12 kJ/(moloC) e 36 kJ/mol.
b) 0,12 kJ/(moloC) e 48 kJ/mol.
c) 0,21 kJ/(moloC) e 36 kJ/mol.
d) 0,21 kJ/(moloC) e 48 kJ/mol.
e) 0,35 kJ/(moloC) e 110 kJ/mol.
 resposta:
resposta:Alternativa A.

próxima »
























































