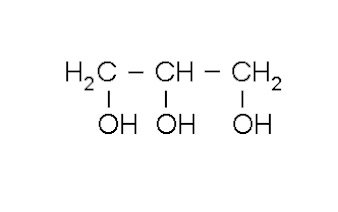Questões de química
Origem: Pucsp
(Pucsp-1996) Considere 4 elementos químicos representados por: X, A, B e C. Sabe-se que:- os elementos A e X pertencem ao mesmo grupo da tabela periódica;
- A, B e C apresentam números atômicos consecutivos, sendo o elemento B um gás nobre.É correto afirmar que:
a) o composto formado por A e C é molecular e sua fórmula é AC.
b) o composto formado por A e C é iônico e sua fórmula é CA.
c) O composto AX apresenta ligação coordenada, sendo sólido a 20°C e 1 atm.
d) Os elementos A e X apresentam eletronegatividades idênticas, por possuírem o mesmo número de elétrons na última camada.
e) C é um metal alcalino-terroso e forma um composto molecular de fórmula CX 2.
resposta:[B]
(Pucsp-1996) A presença de Ozônio na troposfera (baixa atmosfer
a) é altamente indesejável, e seu limite permitido por lei é de 160 microgramas por m¤de ar. No dia 30/07/95, na cidade de São Paulo, foi registrado um índice de 760 microgramas de BaCO
3 por m¤ de ar. Assinale a alternativa que indica quantos mols de BaCO
3 por m¤ de ar, foram encontrados acima do limite permitido por lei, no dia considerado. (Dado:1 micrograma = 10-56g)
a) 1,25.10-5¦ mol
b) 1,25.10-52 mol
c) 1,87.10-5¦ mol
d) 1,87.10-52 mol
e) 2,50.10-5¦ mol
resposta:[A]
(Pucsp-1996) Estudando a deposição eletrolítica dos íons A+Ñ, B+Ò e C+ , foi verificado que a passagem de 4 mols de elétrons pelo circuito provocava a deposição de 4 mols de A, 1 mol de B e 2 mols de C. Os valores de x, Y
2O
3 e t são, respectivamente:
a) 4, 2 e 4
b) 2, 4 e 1
c) 1, 4 e 2
d) 1, 2 e 4
e) 4, 1 e 2
resposta:[C]
(Pucsp-1996) Adicionou-se 100 mL de solução de Hg (NBaCO
3)2 de concentração 0,40 mol/L a 100 mL de solução de Na2S de concentração 0,20 mol/L. Sabendo-se que a reação ocorre com formação de um sal totalmente solúvel (NaNBaCO
3) e um sal praticamente insolúvel (HgS), as concentrações, em mol/L, dos íons Na+ e Hg
2+ presentes na solução final, são respectivamente:
a) 0,1 mol/L e 0,2 mol/L
b) 0,2 mol/L e 0,1 mol/L
c) 0,4 mol/L e 0,2 mol/L
d) 0,4 mol/L e 0,1 mol/L
e) 0,2 mol/L e 0,4 mol/L
resposta:[B]
(Pucsp-1996) Para resolver a questão a seguir utilize-se dos dados a seguir:Combustão do etanol:C
2H
4OH(g) + 3O
2(g) → 2CO
2 (g)+ 3H
2O(g)ΔH de formação de C
2H
4OH(g) = -278 kJ/mol
ΔH de formação de CO
2(g) = -394 kJ/mol
ΔH de formação de H
2O(g) = -286 kJ/mol
ΔH de combustão de óleo BTE = -44 kJ/gPara manter um forno a 1400 °C, uma indústria química queima 1 tonelada por hora de um óleo combustível conhecido por óleo BTE. Caso o combustível fosse substituído por etanol, a massa aproximada desta substância a ser queimada para se obter a mesma quantidade de calor por hora seria:
a) 0,8 ton
b) 1,0 ton
c) 1,5 ton
d) 2,7 ton
e) 3,0 ton
resposta:[C]
(Pucsp-1996) As pilhas de níquel-cádmio têm sido muito usadas na construção de baterias empregadas como fonte de energia, tanto em pequenos aparelhos (calculadoras, brinquedos, telefones sem fio, etc.) como, até mesmo, em satélites espaciais.
Semi-reações, que possivelmente ocorrem nesse, tipo de pilhas alcalinas, estão representadas a seguir:Cd + 2OH →Cd(OH)2 + 2e2Ni(OH)3 + 2e →2Ni(OH)2 + 2OHAssinale a alternativa incorreta:
a) o ΔG do processo é negativo.
b) o cádmio é o pólo negativo da pilha.
c) o Ni(OH)3 constitui o cátodo da pilha.
d) o Cd é o agente redutor e seu número de oxidação aumenta de 0 para +2 no processo direto.
e) os elétrons fluem do eletrodo de Ni (OH)3 para o eletrodo de cádmio.
resposta:[E]
(Pucsp-1996) Uma solução saturada de base, representada por X(OH)2 cuja reação de equilíbrio é: X(OH)2 (s) → X
2+ (aq) + 2OH (aq)tem um pH=10 a 25°C. O produto de solubilidade (Kps) do X(OH)2 é:
a) 5.10-51¤
b) 2.10-51¤
c) 6.10-512
d) 1.10-512
e) 3.10-10
resposta:[A]
(Pucsp-1996) A exposição excessiva ao sol pode trazer sérios danos à pele humana. Para atenuar tais efeitos nocivos, costuma-se utilizar agentes protetores solares, dentre os quais pode-se citar o 2-hidróxi-4-metóxi-benzofenona, cuja fórmula está representada a seguir:
Sobre esta substância é correto afirmar que:
a) apresenta fórmula molecular C10H
4BaCO
3 e é um hidrocarboneto aromático.
b) apresenta fórmula molecular C10H
4O
5e função mista: álcool, éter e cetona.
c) apresenta fórmula molecular C4H2O
5e caráter básico pronunciado pela presença do grupo -OH.
d) apresenta fórmula molecular C4H2BaCO
3 e é um composto aromático de função mista: cetona, fenol e éter.
e) apresenta fórmula molecular C4H603, é totalmente apolar e insolúvel em água.
 resposta:
resposta:[D]
(Pucsp-1996) A glicerina é uma substância utilizada na fabricação de tintas, cosméticos, explosivos, medicamentos, etc. Sua fórmula está representada a seguir:
Em relação à glicerina, assinale a afirmação FALSA:
a) sua combustão completa produz dióxido de carbono e água.
b) reage com ácidos graxos formando gorduras.
c) reage com ácido nítrico produzindo a trinitroglicerina.
d) não apresenta isomeria geométrica (cis/trans).
e) apresenta isomeria óptica por possuir carbono assimétrico.
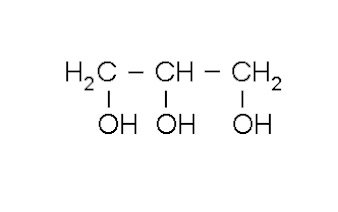 resposta:
resposta:[E]
(Pucsp-1995) Sódio, assim como o hidrogênio, reagem com cloro para formar:
a) um sal e uma base.
b) um composto iônico e um covalente.
c) dois sais.
d) dois compostos iônicos.
e) dois compostos covalentes.
resposta:[B]
(Pucsp-1995) Para a realização de um experimento, será necessário encher de gás um balão de 16,4 L que a 127°C suporta a pressão máxima de 2,0 atm. Nestas condições, a quantidade mais adequada para encher o balão é:
Dados: H = 1, C = 12, 0 = 16 e S = 32, R = 0,082 (atm . L . K-1 . mol-1)
a) 10 g de hidrogênio.
b) 24 g de metano.
c) 45 g de etano.
d) 64 g de dióxido de enxofre.
e) 78 g de acetileno (etino).
resposta:[D]
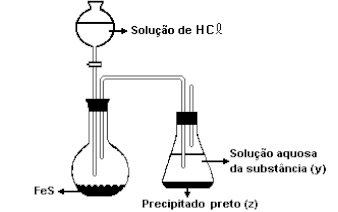
(Pucsp-1995) Considere o aparelho a seguir. Adicionando-se ácido clorídrico ao balão, há uma reação com desprendimento de um gás (x), que ao borbulhar na solução contida no erlenmeY
2O
3er reage, produzindo um precipitado preto (z).
O gás (x), a substância (Y
2O
3) e o precipitado (z) são respectivamente:
a) SO
2Pb(NBaCO
3)2 PbSBaCO
3.
b) SO
2NaNBaCO
3, Na2SBaCO
3.
c) H
2S, Pb(NBaCO
3)2 PbS.
d) H
2S, NaNBaCO
3, Na2S.
e) H
2S, Pb(NBaCO
3)2 Pb(OH)2.
 resposta:
resposta:[C]
(Pucsp-1995) Para a obtenção de 5,2g de sulfito de magnésio foi realizado um processo que constou das seguintes etapas:
(Dados: Mg = 24, O = 16 e S = 32)- combustão de x gramas de enxofre → dióxido de enxofre.
- combustão de Y
2O
3 gramas de magnésio → óxido de magnésio.
- dióxido de enxofre + água → ácido representado por A.
- óxido de magnésio + água → base representada por B.
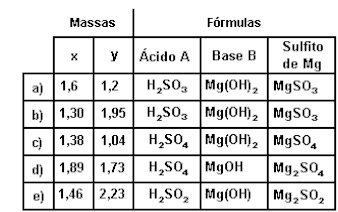
- ácido A + base B → sulfito de magnésio + água.Assinale a alternativa que indica corretamente os valores de x, de Y
2O
3 e as fórmulas do ácido A, da base B e de sulfito de magnésio.
 resposta:
resposta:[A]
(Pucsp-1995) Considerando-se os elementos do 3¡. período da Tabela Periódica, é correto afirmar:
a) o elemento de menor raio atômico é o Na.
b) o elemento de maior potencial de ionização é o Cg.
c) o elemento que reage, violentamente, com água é o de maior número atômico.
d) o elemento que forma com o oxigênio composto iônico de fórmula X
2O é o de menor número atômico.
e) o elemento mais eletronegativo é o Ar.
resposta:[D]
(Pucsp-1995) A massa de NaOH necessária para neutralizar totalmente 200ml de uma solução 0,01 molar de H
2SO
4 é:
(Dados: H = 1; O = 16; Na = 23 e S = 32.)
a) 4,00 g.
b) 2,00 g.
c) 1,60 g.
d) 0,16 g.
e) 0,08 g.
resposta:[D]
(Pucsp-1995) Dentre as alternativas a seguir, é incorreto afirmar que:
a) etanol e etóxi-etano apresentam, respectivamente, isomeria funcional e de compensação.
b) 2-buteno e propino apresentam, respectivamente, reação de adição e de polimerização.
c) fenol e metanóico ionizam em água e são neutralizados por base.
d) por oxidação, 1-propanol fornece propanal e 2-propanol fornece propanona.
e) no etano o número de oxidação de carbono é +3 e no eteno é +2.
resposta:[E]
(Pucsp-1995) A 25°C e 1 atm tem-se:ΔH de formação do CO
2 = - 94,1kcal mol-1
ΔH de formação de H
2O = - 68,3kcal mol-1
ΔH de combustão do C
2H
2 = - 310,6kcal mol-1
ΔS de formação do C
2H
2 = - 0,048kcal mol-1
Escolha entre as alternativas relacionadas na figura a seguir a que completa, adequadamente, a afirmação:A 25°C e 1 atm, ΔH de formação do C
2H
2 é,CH., ΔG é,CH.., portanto o processo é,CH.
 resposta:
resposta:[C]
(Pucsp-1995) Considere o equilíbrio representado por:
Qual dos procedimentos a seguir deslocará o equilíbrio no sentido 1?
a) evaporação da água a uma temperatura fixa.
b) aumento de pressão.
c) adição de benzoato de potássio sólido.
d) adição de ácido sulfúrico.
e) aumento da temperatura da solução.
 resposta:
resposta:[E]
(Pucsp-1995) Para estudar o pH de diferentes sistemas, mantendo-se a temperatura constante, fez-se a seguinte experiência:Em 4 balões volumétricos numerados I, II, III e IV, colocou-se 10mL de diferentes soluções, conforme o indicado a seguir:
balão
I : 10mL de HCl 0,1M
balão
II : 10mL de NaOH 0,1M
balão
III : 10mL de H
3CCOOH 0,1M
balão
IV : 10mL de NH
4OH 0,1M
e adicionou-se água a cada um dos balões, até se obter 1L de solução. Assinale a alternativa que indica, corretamente, o pH encontrado em cada um dos balões:
 resposta:
resposta:[A]
próxima »