Questões de química
Origem: Unirio
(Unirio-1996) Considere que a alga microscópica "Spirulina platensis", muito utilizada como complemento alimentar, possui 48% de carbono e 7% de hidrogênio em massa. Um comprimido dessa alga, comprado em farmácias, possui 1 g de spirulina. Quantos átomos de carbono e de hidrogênio, respectivamente, existem nesse comprimido?Dados:
Constante de Avogadro = 6.10 2¤
Massas Molares: C = 12 g/mol; H = 1 g/mol
a) 2,4 . 1022 e 2,1 . 1022
b) 2,4 . 1022 e 4,2 . 1022
c) 1,2 . 102¤ e 2,1 . 1022
d) 4 e 7
e) 0,04 e 0,07
resposta:[B]
(Unirio-1996) Os sais de Cr 6+ são, em geral, solúveis no pH biológico e, portanto, têm fácil penetração. Daí a sua toxidade para seres humanos. Por outro lado, os compostos de Cr ¤+ são pouco solúveis nesse pH, o que resulta em dificuldade de passar para o interior das células. Indique a opção que corresponde à configuração eletrônica do íon Cr ¤+.
Dado: [Ar] → Argônio (Z = 18)
a) [Ar] 4S
2 3d1
b) [Ar] 3d2
c) [Ar] 3d¤
d) [Ar] 4S
2 3d¥
e) [Ar] 4s1 3d¦
resposta:[C]
(Unirio-1996) Um radioisótopo emite uma partícula ‘ e posteriormente uma partícula ’, obtendo-se ao final o elemento ‰Pa2¤¥. O número de massa e o número atômico do radioisótopo original são, respectivamente:
a) 238 e 92.
b) 237 e 92.
c) 234 e 90.
d) 92 e 238.
e) 92 e 237.
resposta:[A]
(Unirio-1996) Das espécies químicas a seguir, indique aquela que NÃO obedece à regra do octeto.
a) MgBr2
b) Ag Cg
3
c) CO
2
d) NaCg
e) SO
2 resposta:[B]
(Unirio-1996) O consumidor brasileiro já está informado de que os alimentos industrializados que ingere contêm substâncias cuja função básica é a de preservá-los da deterioração. Alguns exemplos dessas substâncias são: conservantes - ácido bórico (P.ll) e anidrido sulfuroso (P.V); antioxidante - ácido fosfórico (A.III); antiumectantes - carbonato de cálcio (Au.l) e dióxido de silício (Au.Vlll). Marque a opção que indica a fórmula de cada substância na ordem apresentada no texto.
a) H
2BO4; SBaCO
3; H
3PBaCO
3; K2CBaCO
3; Si2O
b) H
3BBaCO
3; SO
2; H
3PBaCO
3; K2CBaCO
3; SiO
2
c) H
3BBaCO
3; SO
2; H
3PO4; CaCBaCO
3; SiO
2
d) H
3BBaCO
3; SBaCO
3; H
3PO4; CaCBaCO
3; Si2O
e) H
3BO4; SO
2; H
3PBaCO
3; CaCBaCO
3; SiO
2 resposta:[C]
(Unirio-1996) Óxido de cálcio, óxido de potássio e óxido de sódio reagem separadamente, consumindo 18g de H
2O em cada reação. Considere:m → massa de hidróxido de cálcio formado;
m2 → massa de hidróxido de potássio formado;
m3 → massa de hidróxido de sódio formado.Assim, podemos afirmar que:
Dados:
Massas molares H=1,0g/mol; O=16g/mol; Ca=40g/mol; K=39g/mol; Na=23g/mol
a) m m3 m2
b) m2 m m3
c) m2 m3 m
d) m3 m m2
e) m3 m2 m
resposta:[C]
(Unirio-1996) Ao mergulharmos uma placa de prata metálica em uma solução de ácido nítrico, ocorrerá a seguinte reação: Ag + HNBaCO
3 → AgNBaCO
3 + NO + H
2O
Ajustando a equação química acima, pode-se calcular que a massa de água produzida, quando é consumido 1 mol de prata metálica é, em gramas:
Dado:
Massa molar H
2O = 18 g/mol
a) 36
b) 27
c) 18
d) 12
e) 3,6
resposta:[D]
(Unirio-1996) A seguir é apresentada uma reação química em equilíbrio: 2NO(g) + O
2(g) →2NO
2(g), ΔH < O
Com o objetivo de deslocar esse equilíbrio no sentido da formação de dióxido de nitrogênio, deve-se:
a) diminuir a pressão e a temperatura.
b) aumentar a pressão e a temperatura.
c) aumentar a pressão e diminuir a temperatura.
d) aumentar a pressão e diminuir as concentrações de NO e O
2.
e) aumentar a temperatura e as concentrações de NO e O
2.
resposta:[C]
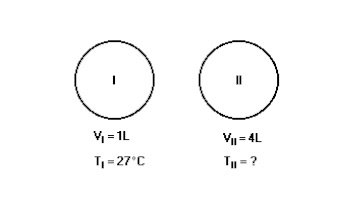
(Unirio-1996) Os dois balões a seguir representados contêm a mesma substância pura na fase gasosa e estão sob a mesma pressão.
Qual a temperatura em Kelvin no balão ll, se ele contém o triplo da massa de gás contida no balão l?
a) 36
b) 127
c) 300
d) 309
e) 400
 resposta:
resposta:[E]
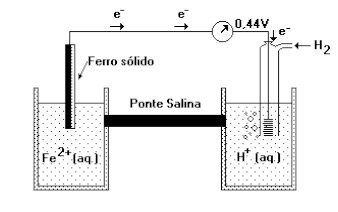
(Unirio-1996) O esquema a seguir representa a pilha ferro-hidrogênio (eletrodo padrão).
O voltímetro indica a força eletromotriz em condições-padrão. O anodo desta pilha e o potencial padrão de redução do ferro são, respectivamente:
a) eletrodo de ferro e - 0,44V
b) eletrodo de ferro e + 0,22V
c) eletrodo de ferro e + 0,44V
d) eletrodo de hidrogênio e - 0,44V
e) eletrodo de hidrogênio e + 0,44V
 resposta:
resposta:[A]
(Unirio-1996) Na reação:
NH
4 + + S
2 → NH
3 + HS,o íon sulfeto (S
2) é uma espécie de característica:
a) básica, segundo a teoria de Bronsted - LowrY
2O
3.
b) básica, segundo a teoria de Arrhenius.
c) ácida, segundo a teoria de Lewis.
d) ácida, segundo a teoria de Bronsted-LowrY
2O
3.
e) ácida, segundo a teoria de Arrhenius.
resposta:[A]
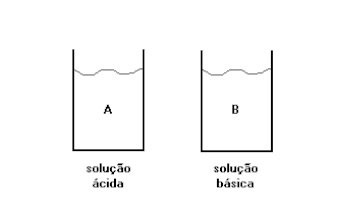
(Unirio-1996) Os recipientes a seguir representam duas soluções aquosas a 25°C.
O valor do pH da solução A (solução ácid
a) é igual ao valor do pOH da solução B (solução básic
a). De acordo com essa informação, podemos afirmar que:
a) pHÛ + pH½ < 14.
b) pHÛ + pH½ = 14.
c) pHÛ + pH½ 14.
d) pOHÛ + pOH½ < 14.
e) pOHÛ + pH½ 14.
 resposta:
resposta:[E]
(Unirio-1996) Num exame laboratorial, foi recolhida uma amostra de sangue, sendo o plasma separado dos eritrócitos, ou seja, deles isolado antes de qualquer modificação fosse feita na concentração de gás carbônico. Sabendo-se que a concentração de CO
2, neste plasma, foi de 0,025 mol/L, essa mesma concentração em g/L, é de:
Dados:
Massas molares C = 12 g/mol; O = 16 g/mol
a) 1760
b) 6.10-6
c) 2,2
d) 1,1
e) 0,70
resposta:[D]
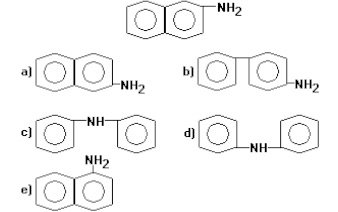
(Unirio-1996) A ’ - naftilamina, cuja fórmula estrutural é apresentada a seguir, é uma substância cancerígena que atua na bexiga humana. O contato com esse tipo de substância é freqüente em pessoas que lidam com certos ramos da indústria química. Assinale a opção que apresenta o isômero plano de posição dessa substância.
 resposta:
resposta:[E]
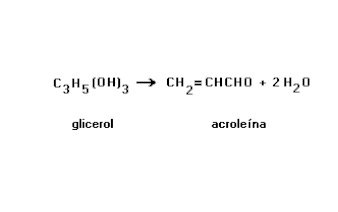
(Unirio-1996) Durante o cozimento da carne, a gordura nela existente produz som ("chiadeira") e aroma peculiares. O glicerol presente na gordura decompõe-se em acroleína (líquido incolor e de forte odor) e água, segundo a reação:
O tipo da reação acima apresentada é:
a) eliminação de aldeídos.
b) eliminação de álcoois.
c) substituição de álcoois.
d) substituição de ácidos.
e) adição de aldeídos
 resposta:
resposta:[B]
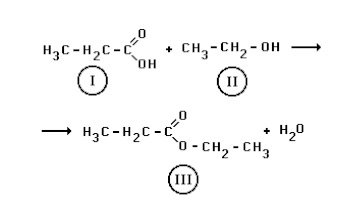
(Unirio-1996) A seguir é apresentada uma reação química onde compostos de diferentes funções orgânicas tomam parte:
Os compostos orgânicos I, II e III pertencem, respectivamente, às seguintes funções orgânicas:
a) aldeído, álcool, éter.
b) aldeído, ácido carboxílico, éster.
c) ácido carboxílico, aldeído, éster.
d) ácido carboxílico, aldeído, éter.
e) ácido carboxílico, álcool, éster.
 resposta:
resposta:[E]
(Unirio-1996) Dois alcenos de fórmula molecular C
5H10 sofrem reações de hidratação em meio ácido. Os produtos principais gerados, respectivamente, são: 3 - metil - 2 - butanol e 2 - metil - 2 - butanol. O tipo de isomeria existente entre os alcenos reagentes e o tipo de isomeria encontrado entre os produtos acima citados são, respectivamente:
a) cadeia e posição.
b) cadeia e cadeia.
c) cadeia e função.
d) posição e posição.
e) função e posição.
resposta:[D]
(Unirio-1996) As reações de substituição do tolueno com Cl
2 podem gerar diferentes produtos, dependendo das condições em que ocorreram. No caso em que esta substituição é realizada com aquecimento e na presença de luz, o produto orgânico formado é:
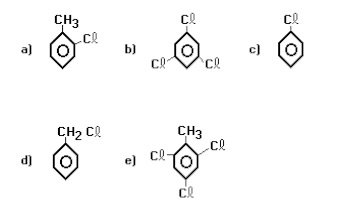 resposta:
resposta:[D]
(Unirio-1996) As reações de combustão parcial e total do metano são, respectivamente:CH
4(g) + 3/2 O
2(g) → CO(g) + 2H
2O(g) ,
sendo ΔH (nas condições padrão)) = - 607,2 kJ/mol; eCH
4(g) + 2O
2(g) → CO
2(g) + 2H
2O(g) , sendo ΔH = XSão os seguintes os valores aproximados dos calores de formação padrão:H
2O (g) → ΔH¡ f = - 285,8 kJ/mol
CO(g) → ΔH¡ f = - 110,5 kJ/mol
CO
2(g) → ΔH¡ f = - 393,5 kJ/molAssim, o valor do ΔH da reação de combustão total (X), em kJ/mol, é, aproximadamente:
a) zero.
b) - 607,2.
c) - 682,1.
d) - 890,2.
e) - 965,1.
resposta:[D]
próxima »







