Questões de química
Tópicos de Química (não classificadas)
(Unesp-2013) (Unesp 2013)

De acordo com as informações do texto, é correto afirmar que
o processo descrito para a obtenção do silício metalúrgico corresponde
a uma reação
(A) endotérmica e de oxirredução, na qual o Si4+ é reduzido
a Si.
(B) espontânea, na qual ocorre a combustão do carbono.
(C) exotérmica, na qual ocorre a substituição do Si por C.
(D) exotérmica, na qual ocorre a redução do óxido de silício.
(E) endotérmica e de dupla troca.
 resposta:
resposta:[A]

(Fuvest-2014) A tabela abaixo apresenta informações sobre cinco gases contidos em recipientes separados e selados.
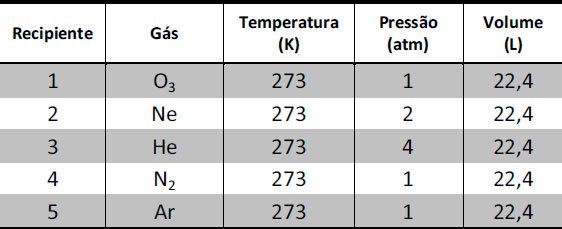
Qual recipiente contém a mesma quantidade de átomos que um recipiente selado de 22,4 L, contendo H2, mantido a 2 atm e 273 K?
a)1
b)2
c)3
d)4
e)5
 resposta:
resposta:C.

(Unesp-2011) O magma que sai dos vulcões durante as erupções é constituído
por rochas fundidas e vários tipos de gases e vapores,
tais como CO, CO2, SO2, SO3, HCl e H2O. A respeito dessas
substâncias, são feitas as seguintes afirmações:
I. Quando dissolvidos em água, os gases CO2, SO2, SO3 e
HCl geram soluções eletrolíticas cujo pH é menor que 7.
II. As moléculas de CO2, SO2 e H2O apresentam geometria
linear.
III. No estado sólido, as moléculas de CO2 encontram-se atraídas
entre si por ligações de hidrogênio muito intensas.
É correto o que se afirma em:
(A) I, apenas.
(B) II, apenas.
(C) I e II, apenas.
(D) II e III, apenas.
(E) I, II e III.
 resposta:
resposta:[A]

(Fuvest-2014) No processo tradicional, o etanol é produzido a partir do caldo da cana-de-açúcar por fermentação promovida por leveduras naturais, e o bagaço
de cana é desprezado.
Atualmente, leveduras geneticamente modificadas podem ser utilizadas em novos processos de fermentação para a produção de biocombustíveis. Por
exemplo, no processo A, o bagaço de cana, após hidrólise da celulose e da hemicelulose, também pode ser transformado em etanol.
No processo B, o caldo de cana, rico em sacarose, é transformado em farneseno que, após hidrogenação das ligações duplas, se transforma no
"diesel de cana". Esses três processos de produção de biocombustíveis podem ser representados por:
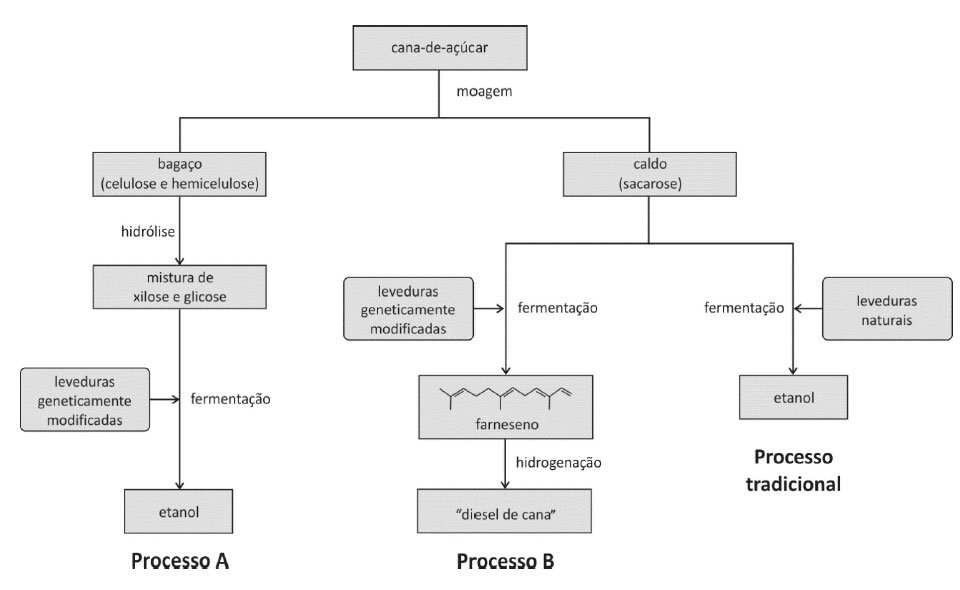
Com base no descrito acima, é correto afirmar:
a)No Processo A, a sacarose é transformada em celulose por micro-organismos transgênicos.
b)O Processo A, usado em conjunto com o processo tradicional, permite maior produção de etanol por hectare cultivado.
c)O produto da hidrogenação do farneseno não deveria ser chamado de “diesel”, pois não é um hidro caboneto,
d)A combustão do etanol produzido por micro-orgnismos transgênicos não é poluente, pois não produz dióxido de carbono.
e)O Processo B é vantajoso em relação ao Processo A, pois a sacarose é matéria-prima com menor valor ecnômico do que o bagaço de cana.
 resposta:
resposta:B.

(Fuvest-2011) As fórmulas estruturais de alguns componentes de
óleos essenciais, responsáveis pelo aroma de certas
ervas e flores, são:
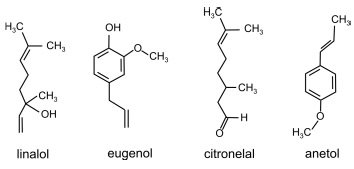
Dentre esses compostos, são isômeros:
a) anetol e linalol.
b) eugenol e linalol.
c) citronelal e eugenol.
d) linalol e citronelal.
e) eugenol e anetol.
 resposta:
resposta:[D]

(Unesp-2013) (Unesp 2013)Instrução: Leia o texto para responder às questões de números
70 e 71.
O silício metalúrgico, purificado até atingir 99,99% de
pureza, é conhecido como silício eletrônico. Quando cortado
em fatias finas, recobertas com cobre por um processo eletrolítico
e montadas de maneira interconectada, o silício eletrônico
transforma-se em microchips.
A figura reproduz uma das últimas etapas da preparação
de um microchip.
As fatias de silício são colocadas numa solução
de sulfato de cobre. Nesse processo, íons de cobre
deslocam-se para a superfície da fatia (cátodo), aumentando
a sua condutividade elétrica.
(http://umumble.com. Adaptado.)

O processo de recobrimento das fatias de silício é conhecido
como
(A) eletrocoagulação.
(B) eletrólise ígnea.
(C) eletrodeformação.
(D) galvanoplastia.
(E) anodização.
 resposta:
resposta:[D]

(Unesp-2013) (Unesp 2013)Instrução: Leia o texto para responder às questões de números
70 e 71.
O silício metalúrgico, purificado até atingir 99,99% de
pureza, é conhecido como silício eletrônico. Quando cortado
em fatias finas, recobertas com cobre por um processo eletrolítico
e montadas de maneira interconectada, o silício eletrônico
transforma-se em microchips.
A figura reproduz uma das últimas etapas da preparação
de um microchip.
As fatias de silício são colocadas numa solução
de sulfato de cobre. Nesse processo, íons de cobre
deslocam-se para a superfície da fatia (cátodo), aumentando
a sua condutividade elétrica.
(http://umumble.com. Adaptado.)

A semirreação na superfície da fatia de silício, cátodo, é representada
por:
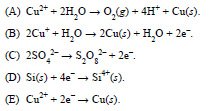
 resposta:
resposta:[E]

(Fuvest-2014) Uma embalagem de sopa instantânea apresenta, entre outras, as seguintes informações: “Ingredientes: tomate, sal, amido, óleo vegetal,
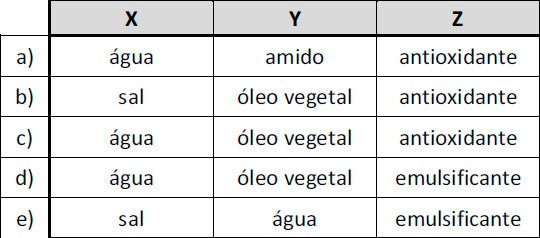
emulsificante, conservante, flavorizante, corante, antioxidante”. Ao se misturar o conteúdo da embalagem com água quente, poderia ocorrer a
separação dos componentes X e Y da mistura, formando duas fases, caso o ingrediente Z não estivesse presente.
Assinale a alternativa em que X, Y e Z estão corretamente identificados.
 resposta:
resposta:B.

(Enem-2013) (Enem 2013) Uma das etapas do tratamento de água é a desinfecção, sendo a cloração o método mais
empregado. Esse método consiste na dissolução dos gás cloro numa solução sob pressão e
sua aplicação na água a ser desinfectada. As equações das reações químicas envolvidas são:

A ação desinfetante é controlada pelo ácido hipocloroso, que possui um potencial de
desinfecção cerca de 80 vezes superior ao ânion hipoclorito. O pH do meio é importante,
porque influencia na extensão com que o ácido hipocloroso se ioniza.
Para que a desinfecção seja mais efetiva, o pH da água a ser tratada deve estar mais próximo
de
A) 0.
B) 5.
C) 7.
D) 9.
E) 14
 resposta:
resposta:B.

(Fuvest-2011) Em cadeias carbônicas, dois átomos de carbono
podem formar ligação simples (C?C), dupla (C?C) ou
tripla (C?C). Considere que, para uma ligação simples,
a distância média de ligação entre os dois átomos de
carbono é de 0,154 nm, e a energia média de ligação é
de 348 kJ/mol.
Assim sendo, a distância média de ligação (d) e a
energia média de ligação (E), associadas à ligação
dupla (C?C), devem ser, respectivamente,
a) d < 0,154 nm e E > 348 kJ/mol.
b) d < 0,154 nm e E < 348 kJ/mol.
c) d = 0,154 nm e E = 348 kJ/mol.
d) d > 0,154 nm e E < 348 kJ/mol.
e) d > 0,154 nm e E > 348 kJ/mol.
 resposta:
resposta:[A]

(Fuvest-2014) Em um laboratório químico, um estudante encontrou quatro frascos (1, 2, 3 e 4) contendo soluções aquosas incolores de sacarose, KCl, HCl e
NaOH, não necessariamente nessa ordem. Para identificar essas soluções, fez alguns experimentos simples, cujos resultados são apresentados na
tabela a seguir:

As soluções aquosas nos frascos 1, 2, 3 e 4 são, respectivamente, de
a)HCl, NaOH, KCl e sacarose.
b)KCl, NaOH, HCl e sacarose.
c)HCl, sacarose, NaOH e KCl.
d)KCl, sacarose, HCl e NaOH.
e)NaOH, HCl, sacarose e KCl.
 resposta:
resposta:B.

(Enem-2013) (Enem 2013) Em um experimento foram utilizadas duas garrafas PET, uma pintada de branco e a outra de preto, acopladas
cada uma a um termômetro. No ponto médio da distância entre as garrafas, foi mantida acesa, durante
alguns minutos, uma lâmpada incandescente. Em seguida a lâmpada foi desligada. Durante o experimento,
foram monitoradas as temperaturas das garrafas: a) enquanto a lâmpada permaneceu acesa e b) após a lâmpada
ser desligada e atingirem equilíbrio térmico com o ambiente.

A taxa de variação da temperatura da garrafa preta, em comparação à da branca, durante todo experimento,
foi
A) igual no aquecimento e igual no resfriamento.
B) maior no aquecimento e igual no resfriamento.
C) menor no aquecimento e igual no resfriamento.
D) maior no aquecimento e menor no resfriamento.
E) maior no aquecimento e maior no resfriamento.
 resposta:
resposta:E

(Enem-2013) (Enem 2013) O brasileiro consome em média 500 miligramas de cálcio por dia, quando a quantidade recomendada é o
dobro. Uma alimentação balanceada é a melhor decisão pra evitar problemas no futuro, como a osteoporose,
uma doença que atinge os ossos. Ela se caracteriza pela diminuição substancial de massa óssea, tornando os
ossos frágeis e mais suscetíveis a fraturas.
Disponível em: www.anvisa.gov.br. Acesso em: 1 ago. 2012 (adaptado).
Considerando-se o valor de 6 x 1023 mol-1 para a constante de Avogadro e a massa molar do cálcio igual a
40 g/mol, qual a quantidade mínima diária de átomos de cálcio a ser ingerida para que uma pessoa supra
suas necessidades?

 resposta:
resposta:B

(Unesp-2013) (Unesp 2013)Instrução: Leia o texto para responder às questões de números
72 a 74.
Alguns cheiros nos provocam fascínio e atração. Outros
trazem recordações agradáveis, até mesmo de momentos da
infância. Aromas podem causar sensação de bem-estar ou dar
a impressão de que alguém está mais atraente. Os perfumes
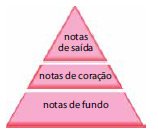
têm sua composição aromática distribuída em um modelo conhecido
como pirâmide olfativa, dividida horizontalmente em
três partes e caracterizada pelo termo nota. As notas de saída,
constituídas por substâncias bem voláteis, dão a primeira impressão
do perfume. As de coração demoram um pouco mais
para serem sentidas. São as notas de fundo que permanecem
mais tempo na pele.
(Cláudia M. Rezende. Ciência Hoje, julho de 2011. Adaptado.)
À temperatura e pressão ambientes, os constituintes químicos
das notas de saída
(A) são líquidos oleosos que aderem à pele por meio de ligações
de hidrogênio.
(B) evaporam mais rapidamente que os constituintes químicos
das notas de coração e de fundo.
(C) apresentam densidade mais elevada que os constituintes
químicos das notas de coração e de fundo.
(D) são gases cujas moléculas possuem elevada polaridade.
(E) são pouco solúveis no ar atmosférico.
 resposta:
resposta:[B]

(Unesp-2013) (Unesp 2013)Instrução: Leia o texto para responder às questões de números
72 a 74.
Alguns cheiros nos provocam fascínio e atração. Outros
trazem recordações agradáveis, até mesmo de momentos da
infância. Aromas podem causar sensação de bem-estar ou dar
a impressão de que alguém está mais atraente. Os perfumes
têm sua composição aromática distribuída em um modelo conhecido
como pirâmide olfativa, dividida horizontalmente em
três partes e caracterizada pelo termo nota. As notas de saída,
constituídas por substâncias bem voláteis, dão a primeira impressão
do perfume. As de coração demoram um pouco mais
para serem sentidas. São as notas de fundo que permanecem
mais tempo na pele.
(Cláudia M. Rezende. Ciência Hoje, julho de 2011. Adaptado.)

Um químico, ao desenvolver um perfume, decidiu incluir
entre os componentes um aroma de frutas com concentração
máxima de 10–4mol/L. Ele dispõe de um frasco da substância
aromatizante, em solução hidroalcoólica, com concentração de
0,01 mol/L.
Para a preparação de uma amostra de 0,50 L do novo perfume,
contendo o aroma de frutas na concentração desejada, o volume
da solução hidroalcoólica que o químico deverá utilizar
será igual a
(A) 5,0 mL.
(B) 2,0 mL.
(C) 0,50 mL.
(D) 1,0 mL.
(E) 0,20 mL.
 resposta:
resposta:[A]

(Enem-2013) (Enem 2013) O uso de embalagens plásticas descartáveis vem crescendo em todo o mundo, juntamente com o problema
ambiental gerado por seu descarte inapropriado. O politereftalato de etileno (PET), cuja estrutura é mostrada,
tem sido muito utilizado na indústria de refrigerantes e pode ser reciclado e reutilizado. Uma das opções
possíveis envolve a produção de matérias-primas, como o etilenoglicol (1,2-etanodiol), a partir de objetos
compostos de PET pós-consumo.

Com base nas informações do texto, uma alternativa para a obtenção de etilenoglicol a partir do PET é a
A) solubilização dos objetos.
B) combustão dos objetos.
C) trituração dos objetos.
D) hidrólise dos objetos.
E) fusão dos objetos.
 resposta:
resposta:D

(Fuvest-2011) Para investigar o fenômeno de oxidação do ferro,
fez-se o seguinte experimento: No fundo de cada um de
dois tubos de ensaio, foi colocada uma amostra de fios
de ferro, formando uma espécie de novelo. As duas
amostras de ferro tinham a mesma massa. O primeiro
tubo foi invertido e mergulhado, até certa altura, em um
recipiente contendo água. Com o passar do tempo,
observou-se que a água subiu dentro do tubo, atingindo
seu nível máximo após vários dias. Nessa situação,
mediu-se a diferença (x) entre os níveis da água no tubo
e no recipiente. Além disso, observou-se corrosão
parcial dos fios de ferro. O segundo tubo foi mergulhado
em um recipiente contendo óleo em lugar de água.
Nesse caso, observou-se que não houve corrosão
visível do ferro e o nível do óleo, dentro e fora do tubo,
permaneceu o mesmo.

Sobre tal experimento, considere as seguintes
afirmações:
I. Com base na variação (x) de altura da coluna de
água dentro do primeiro tubo de ensaio, é possível
estimar a porcentagem de oxigênio no ar.
II. Se o experimento for repetido com massa maior de
fios de ferro, a diferença entre o nível da água no
primeiro tubo e no recipiente será maior que x.
III. O segundo tubo foi mergulhado no recipiente com
óleo a fim de avaliar a influência da água no
processo de corrosão.
Está correto o que se afirma em
a) I e II, apenas.
b) I e III, apenas.
c) II, apenas.
d) III, apenas.
e) I, II e III.
 resposta:
resposta:[B]

(Unesp-2013) (Unesp 2013)Instrução: Leia o texto para responder às questões de números
72 a 74.
Alguns cheiros nos provocam fascínio e atração. Outros
trazem recordações agradáveis, até mesmo de momentos da
infância. Aromas podem causar sensação de bem-estar ou dar
a impressão de que alguém está mais atraente. Os perfumes
têm sua composição aromática distribuída em um modelo conhecido
como pirâmide olfativa, dividida horizontalmente em
três partes e caracterizada pelo termo nota. As notas de saída,
constituídas por substâncias bem voláteis, dão a primeira impressão
do perfume. As de coração demoram um pouco mais
para serem sentidas. São as notas de fundo que permanecem
mais tempo na pele.
(Cláudia M. Rezende. Ciência Hoje, julho de 2011. Adaptado.)

A B-ionona é uma substância química de vasta aplicação na
perfumaria, em produtos cuja fórmula requer aroma floral.

A substância química B-ionona
(A) apresenta, em soluções aquosas, atividade óptica.
(B) reage com água, formando diois vicinais.
(C) contém três grupos metila, ligados a átomos de carbono
idênticos.
(D) contém duplas ligações conjugadas.
(E) possui grupos funcionais com propriedades oxidantes.
 resposta:
resposta:[D]

(Unesp-2013) (Unesp 2013)

 resposta:
resposta:[C]

próxima »